Us wichtichste produkten: Aminosilikon, bloksilikon, hydrofile silikon, al har silikonemulsie, ferbettermiddel foar it bevochtigjen fan wriuwfêstens, wetterôfstjittend (fluorfrij, koalstof 6, koalstof 8), deminewaskgemyske stoffen (ABS, enzym, spandexbeskermer, mangaanferwiderer), foar mear details nim dan kontakt op mei: Mandy +86 19856618619 (Whatsapp)
Ynlieding ta surfactants
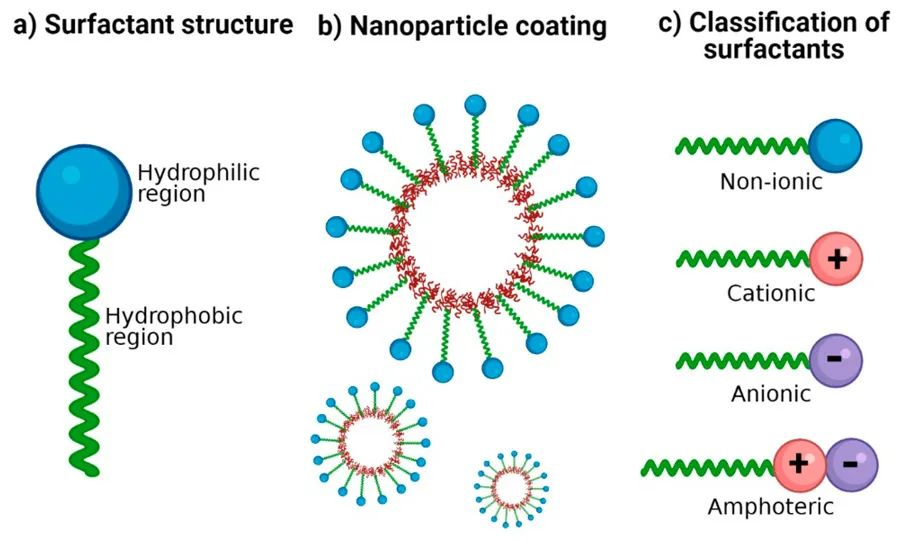
Surfactanten hawwe in amfifilyske molekulêre struktuer: it iene ein befettet in hydrofile groep, de hydrofile kop neamd, wylst it oare ein in hydrofobe groep befettet, de hydrofobe sturt. De hydrofile kop lit surfactanten oplosse yn wetter yn har monomeerfoarm.
De hydrofile groep is faak in poalgroep, dy't in karboksylgroep (-COOH), in sulfonsoergroep (-SO3H), in aminogroep (-NH2), aminen en harren sâlt, hydroksylgroepen (-OH), amidegroepen of etherferbiningen (-O-) kin wêze as oare foarbylden fan poalhydrofile groepen.
De hydrofobe groep is typysk in net-polare koalwetterstofketen, lykas hydrofobe alkylketens (R- foar alkyl) of aromatyske groepen (Ar- foar aryl).
Surfaktanten kinne wurde kategorisearre yn ionyske surfaktanten (ynklusyf kationyske en anionyske surfaktanten), net-ionyske surfaktanten, amfotere surfaktanten, mingde surfaktanten, en oaren. Yn surfaktantoplossingen, as de konsintraasje fan 'e surfaktant in bepaalde wearde berikt, sille surfaktantmolekulen ferskate oardere aggregaten foarmje, bekend as micellen. It proses fan micellisaasje, of micelfoarming, is in krúsjale fûnemintele eigenskip fan surfaktantoplossingen, om't in protte wichtige tuskenflakferskynsels ferbûn binne mei de foarming fan micellen.
De konsintraasje wêrby't surfactants micellen foarmje yn oplossing wurdt oantsjut as de Krityske Micellekonsintraasje (CMC). Micellen binne gjin fêste, sferyske struktueren; leaver, se litte ekstreme ûnregelmjittichheid en dynamyske foarmferoarings sjen. Under bepaalde omstannichheden kinne surfactants ek omkearde micelle-tastannen sjen litte.
Faktoaren dy't ynfloed hawwe op CMC:
- Struktuer fan 'e surfactant
- Type en oanwêzigens fan tafoegings
- Temperatuer
Ynteraksjes tusken surfactants en proteïnen
Proteïnen befetsje net-polare, polare en laden groepen, en in protte amfifilike molekulen kinne op ferskate manieren mei proteïnen ynteraksje hawwe. Ofhinklik fan 'e omstannichheden kinne surfactants molekulêr organisearre aggregaten foarmje mei ferskillende struktueren, lykas micellen of omkearde micellen, dy't oars ynteraksje hawwe mei proteïnen.
De ynteraksjes tusken proteïnen en surfactants (Proteïne-Surfactant, PS) omfetsje benammen elektrostatyske ynteraksjes en hydrofobe ynteraksjes. Ionyske surfactants ynteraksje mei proteïnen benammen troch de elektrostatyske krêften fan 'e poalgroep en de hydrofobe ynteraksjes fan 'e alifatyske koalstofketen, wêrby't se binde oan 'e poal- en hydrofobe regio's fan it proteïne, en sa PS-kompleksen foarmje.
Net-ionogene surfactants ynteraksje primêr mei proteïnen fia hydrofobe krêften, wêrby't de hydrofobe keatlingen ynteraksje hawwe mei de hydrofobe regio's fan 'e proteïnen. De ynteraksje kin sawol de struktuer as de funksje fan 'e surfactant as it proteïne beynfloedzje. Dêrom bepale it type en de konsintraasje fan surfactants, tegearre mei de miljeukontekst, oft surfactants proteïnen stabilisearje of destabilisearje, en ek oft se aggregaasje of fersprieding befoarderje.
HLB-wearde fan surfactants
Foar in surfactant om syn unike ynterfaciale aktiviteit te fertoanen, moat it de hydrofobe en hydrofile komponinten yn lykwicht hâlde. De HLB (Hydrophile-Lipophile Balance) is in mjitte fan 'e hydrofile-lipofile lykwicht fan surfactants en tsjinnet as in yndikator fan 'e hydrofile en hydrofobe eigenskippen fan' e surfactants.
De HLB-wearde is in relative wearde (fariearjend fan 0 oant 40). Bygelyks, paraffine hat in HLB-wearde fan 0 (gjin hydrofile komponint), polyethyleenglycol hat in HLB-wearde fan 20, en de tige hydrofile SDS (natriumdodecylsulfaat) hat in HLB-wearde fan 40. De HLB-wearde kin tsjinje as in rjochtlinige referinsje by it selektearjen fan surfactants. In hegere HLB-wearde jout bettere hydrofilisiteit oan, wylst in legere HLB-wearde in mindere hydrofilisiteit suggerearret.
Pleatsingstiid: 10 septimber 2024

